Qu'est-ce que le clonage ?
Pour commencer nous allons donner la définition du clonage tirée du dictionnaire Le petit Larousse 1998 : "obtention par des manipulations biologiques d'une série de molécules identiques (acide nucléique) ou de cellules isolées d'êtres unicellulaires (bacteries) et d'êtres pluricellulaires (amphibiens , mammifères) au patrimoine génétique identique."
La technique de clonage que nous allons étudier est le clonage dit somatique qui consiste grossièrement, à prélever sur un mammifère adulte n'importe quelle cellule de l'organisme (hormis les cellules nerveuses) pour l'introduire dans un ovocyte auparavant privé de son matériel génétique par énucléation (ablation de son noyau). Cependant cette technique s'avère en réalité plus complexe.
En effet, de nombreux facteurs interviennent dans le déroulement de cette manipulation que nous allons détailler, schémas à l'appui.
L'ENUCLEATION DE L'OVOCYTE
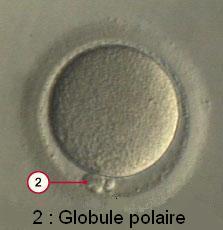
Tout d'abord il faut savoir que l'ablation du matériel génétique de l'ovocyte ne peut se faire que pendant un laps de temps appelé métaphase II; de plus à chaque tentative de clonage il faut prélever plusieurs centaines d'ovocytes car le taux de réussite (% d'ovocyte aboutissant à un clone suite à des manipulations que nous allons détailler) est peu élevé. Lorsque l'ovocyte est en métaphase II (une des phases de la méiose) un élément appelé globule polaire est visible (2), cet élement contient la moitié du patrimoine génétique de l'ovocyte. Lorsque celui-ci est visible cela veut dire que le patrimoine génétique de l'ovocyte est en train de se diviser en deux parties (une moitié allant dans le globule polaire qui sera par la suite libéré par l'ovocyte et l'autre moitié restant dans l'ovocyte). Quand le globule polaire est en formation, le patrimoine génétique de l'ovocyte est regroupé près de la membrane. Il s'agit donc du moment le plus aisé pour faire l'ablation du matériel génétique de l'ovocyte par micro-aspiration.
Photographie d'un globule polaire(accroché à son ovocyte)
Les manipulations se font sous microscope
Pour mettre en évidence les chromosomes dont on veut faire l'ablation, on peut utiliser différentes substances comme l'iodure de propidium, le bromure d’éthidium ou le hoescht. Toutes ces substances ont la particularité de se fixer à l'ADN et, lorsqu'elles sont soumises à un rayonnement UV, sont fluorescentes. Ainsi, pour identifier les chromosomes que l'on doit enlever on asperge l'ovocyte d'une de ces substances.
Effet de la coloration de Hoescht sur l'ADN après exposition à un rayonnement UV
Après avoir aspergé l'ovocyte de colorant de hoescht (ou une des autres solutions précedemment citées), il faut de nouveau lui administrer une drogue permettant à sa zone pellucide (zone de l'ovule entourant le cytoplasme) d'être plus souple dans le but de faciliter la pénétration d'une micropipette. En effet, après la mise en évidence des chromosomes de l'ovocyte grâce à l'effet des rayonnements UV sur le colorant de hoescht, on peut procéder à l'ablation du globule polaire et du matériel génétique de l'ovocyte par l'utilisation d'une micropipette (15 microns de diamètre environ) :
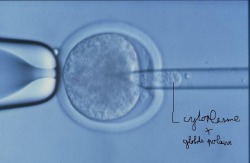
Pénétration de la micropipette qui prélève du cytoplasme (contenant les chromosomes de l'ovocyte) ainsi que le globule polaire.
On voit sur la photographie du haut la micropipette en train de prélever par micro aspiration un peu du cytoplasme de l'ovocyte contenant le matériel génétique de cette dernière ainsi que le globule polaire.
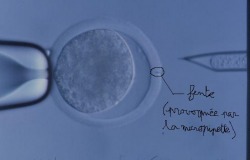
On peut observer sur cette photographie que le volume du cytoplasme de l'ovocyte a diminué suite au prélèvement de la micropipette. On peut voir également la fente qu'a provoqué la pénétration de la micropipette.
Vidéo présentant l'énucléation d'un ovocyte (la coloration bleue provient de l'effet des ultraviolets sur le colorant de hoecsht pour mettre en évidence les chromosomes ).
NB: sur cette vidéo le globule polaire n'est pas extrait de l'ovocyte.
Nous allons maintenant développer l'étape suivant l'énucléation de l'ovocyte : le transfert de noyau.
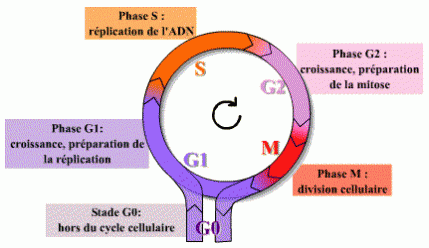
Il faut avant toute chose préciser que pour des raisons de techniques on transfère une cellule entière (membrane + cellule +cytoplasme) dans l'ovocyte énucléée et non pas seulement un noyau car, ce dernier étant très petit il est difficile de le sortir de sa cellule pour le transférer dans l'ovocyte énucléé. De plus, pour plus de facilité on utilise des cellules de peau appelées fibroblaste comme cellule donneuse. En effet, ces fibroblastes (issues dans la quasi-totalité des cas d'animaux adultes) sont très souvent utilisés au vue de la facilité que l'on a à les prélever et à les maintenir en culture in vitro (voir infra). Pour commencer, il faut prélever sur un animal adulte plusieurs centaines de fibroblastes (de peau en général); celles-ci ont été prises, concernant Dolly (premier mammifère cloné), à un des stades du cycle cellulaire appelé G0 (voir schéma) qui est situé en dehors du cycle de division.
Cycle cellulaire
Ce stade G0 a été choisi car on croyait qu'à cet instant précis, le noyau avait le plus de chances de se reprogrammer après son injection dans l'ovocyte (qui lui est en métaphase 2). Ce stade correspond également au dernier de la vie de la cellule ; cette dernière va commencer à "mourir" une fois son entrée dans ce stade, la cellule est dans un état de quiescence ( elle est très peu active). En résumé , les cellules donneuses étaient prélevées alors qu'elles allaient bientôt "mourir". Actuellement, en France on choisit plutôt le stade G2 après s'être rendu compte que le clonage était possible à tous les stades du cycle cellulaire.
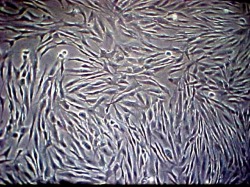
Fibroblastes dans leur milieu de culture (forme allongée)
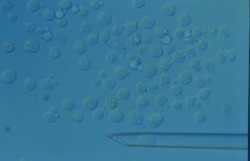
Pour obtenir la forme sphérique des fibroblastes comme dans la photographie ci-dessous, on soumet les fibroblastes à la forme allongée (voir ci-dessus) à une enzyme chargée de séparer les cellules et d'arrondir leur forme.
Fibroblastes de peau après action de l'enzyme
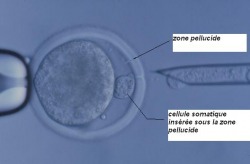
Une fois ces cellules modifiées, elles deviennent plus faciles à manipuler. Elles peuvent être également congelées, décongelées, recongelées sans dommage. Après avoir subi l'effet de l'enzyme, la cellule peut être injectée dans l'ovocyte énucléé. Pour cela, on place le fibroblaste dans une micropipette qui servira à l'injecter dans l'ovocyte et plus particulièrement sous la zone pellucide :
Cellule somatique injectée sous la zone pellucide de l'ovocyte.
Transfert d'une cellule de peau (fibroblaste) dans un ovocyte énucléé.
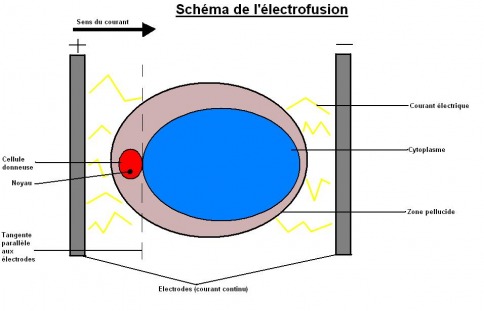
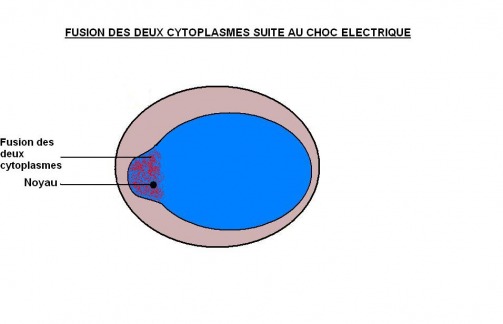
Une fois ce transfert réalisé, on va faire fusionner entre eux l'ovocyte énucléés et la cellule donneuse. Pour ce faire, on applique à l'ensemble ovocyte-fibroblaste un choc électrique (courant continu) d'une très faible tension de l'ordre du millivolt pendant quelques microsecondes : c'est l'électrofusion. Celle ci va donc permettre à la membrane de la cellule donneuse de fusionner avec l'ovocyte. Cette électrofusion a également pour but de simuler le choc que produit sur l'ovocyte le spermatozoïde lors d'une reproduction naturelle, c'est donc ce choc qui va en partie mettre en route le processus de divison cellulaire dans l'ovocyte (dont l'activité sera, par ce choc, en partie activée). En effet, il existe un autre facteur permettant l'activation de l'ovocyte et donc, la division cellulaire de la cellule embryonnaire obtenue par la fusion de l'ovocyte et de la cellule de peau (fibroblastes). Nous l'évoquerons après ces schémas expliquant l'électrofusion.
En métaphase 2, le niveau de MPF (Maturation Promoting Factor) est élevé. C'est cet élément qui est décisif dans la fusion et la reprogrammation du noyau de la cellule donneuse en noyau ressemblant à un noyau de stade embryonnaire "totipotent" pouvant permettre la division de la cellule engendrant un organisme entier. En effet, la cellule "donneuse" est spécialisée cela veut dire qu'elle ne sait assurer qu'une seule fonction (faire de la peau pour une cellule de peau, faire du lait pour une cellule mammaire...).
Cette spécialisation est dûe au fait que l'ADN de la cellule est condensé d'une telle façon que l'ARN polymérase ne pourra accéder qu'à certaines parties de cet ADN. On obtiendra ainsi de l'ARN messager qui ne correspond qu'aux parties "accessibles". La cellule n'a donc "accès" qu' à une minorité du patrimoine génétique qui est dans son noyau. Lors du choc électrique, l'activité de MPF est déclenchée, c'est elle qui va provoquer la dégradation de la membrane nucléaire faisant ainsi fusionner les deux cytoplasmes entre eux .
Ce MPF aura aussi pour fonction de décondenser la chromatine du noyau et va déclencher le début des divisions cellulaires qu'on appelle la mitose. Puis peu de temps après, il va disparaître. On notera que le respect du "timing" de l'expérience est crucial en vue des changements qui sont très rapides et de leur importance. Cette chromatine va donc se décondenser et l'ARN polymérase aura ainsi accès à tout le patrimoine génétique (lors d'une expérience réussie). La cellule est ainsi déspécialisée.
On a ainsi obtenu un noyau ressemblant à celui d'un ovocyte, et ayant les mêmes fonctions que celui d'une cellule embryonnaire totipotente qui peut ainsi se diviser.Nous avons donc maintenant obtenu un ovocyte ayant le même patrimoine génétique que celui de la cellule donneuse.
La cellule embryonnaire obtenue sera ensuite cultivée in vitro dans un milieu de culture à 38.5°C(tempéraure consigne chez le bovin) qui lui permettra de se diviser. Ce milieu de culture voit son atmosphère contrôlée en CO2 et composé de produits tels que le CR1AA le KSOM ou le SOF qui vont permettre à la l'embryon de se développer correctement. Il est possible de pratiquer la coculture avec d'autres cellules appelées Véro qui sécrètent des facteurs de croissance nécessaires au développement de l'embryon dans le milieu.
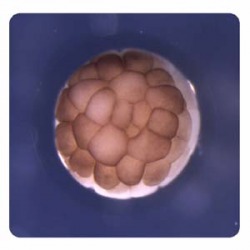
La cellule va donc se diviser au bout de 7 jours si la division ne s'est pas stoppée (mauvaise reprogrammation du noyau par exemple) elle aura atteint le stade blastocyste aussi appelé blastula (128 cellules ). On pourra alors l'introduire dans l'utérus d'une mère porteuse par voies naturelles. On aura ensuite obtenu après les 9 mois de gestation de la vache un clone.
cellule au stade blastula (128 cellules)
Nous vous invitons maintenant à consulter la deuxième partie de notre exposé sur les applications du clonage somatique : le clonage reproductif.