Les limites techniques
Dans les précédentes parties, nous avons vu en quoi consistait le clonage ainsi que ses différentes applications. Dans cette troisième partie, nous allons développer les principales limites techniques du clonage.Les succès du clonage sont très limités : on constate que seuls 1 à 7 % (selon les méthodes) des embryons clonés aboutisssent à des animaux viables.
On peut donc dire que le clonage a un rendement très faible. Le rendement étant caractérisé par le nombre de clones obtenus après toute la série de manipulations. Cela nous amène ainsi à nous demander quelles en sont les causes.
Tout d'abord, cela peut s'expliquer par des manipulations difficiles. En effet, comme nous l'avons vu dans les précédentes parties, il faut retirer le noyau de l'ovule sans la déteriorer ce qui s'avère ardu compte tenu du diamètre de l'ovule (0.2 mm pour un humain). Le moindre faux mouvement peut donc faire échouer la manipulation. De plus, l'approvisionnement en ovules pose problème car il en faut en grand nombre pour les expériences. Par exemple pour la célèbre brebis Dolly, il a fallu pas moins de 1000 ovules pour qu'elle voie le jour. Cependant, ces problèmes sont humains et matériels ce qui n'explique pas pour autant ce taux si élevé d'échecs. Il y a donc d'autres facteurs expliquant ces derniers.
L'un de ceux-ci est appelé "reprogrammation". Lorsque l'on prélève une cellule du corps donneur, celle-ci est spécialisée. Par exemple une cellule de peau est spécialisée dans la fonction "fabrication d'épiderme" et ne sait pas faire autre chose car la partie de son patrimoine génétique concernant la fabrication d'épiderme est activée alors que les autres parties de son patrimoine génétique sont silencieuses : elles sont présentes mais ne s'expriment pas. Cela est dû au fait que la chromatine des cellules de peau est condensée de manière que l'ARN polymérase ne pourra accéder qu'aux parties de l'ADN qui contiennent les informations nécessaires à la création de cellule de peau.
Pour que le clonage fonctionne, il faut que cette cellule se "déspécialise", se "reprogramme" afin que son noyau se comporte comme un noyau d'embryon. Le problème vient du fait qu'à l'heure actuelle ce phénomène est mal compris. Cette reprogrammation est possible grâce à des MPF présents dans l'ovule qui décondensent la chromatine. Le problème se trouve à ce niveau : il arrive que la chromatine ne se décondense pas correctement et que certaines parties de l'ADN restent inaccessibles à l'ARN polymérase. A ce moment, soit la division cellulaire s'arrête soit le clone n'est pas viable.
Ensuite, lorsque l'on parle du clonage, on s'attend a avoir deux êtres strictiment identiques; or deux clones ne sont pas identiques en tout point. Il ne s'agit pas réellement d'une limite qui pose un problème mais le fait que les clones ne soient pas exactement pareils que le donneur de cellule montre que le clonage ne permet pas de reproduire un animal à l'identique. Ainsi certains veaux clonés n'ont pas les mêmes taches sur leur robe que l'animal qui a été cloné. Cette différence peut s'expliquer par l'alimentation de la mère porteuse; malgré tout, la surface totale de taches est la même pour le clone et le cloné.
De plus, l’ADN mitochondrial transmis par la mère (l’ovocyte receveur) est différent d’un clone à l’autre : il est issu du cytoplasme de chacun des ovules utilisés pour reprogrammer l’activité du noyau de chaque cellule donneuse. Les clones ne sont donc pas génétiquement identiques mais extrêmement proches.
Ensuite, un autre problème vient du placenta de la mère et du futur clone qui dans certains cas ont un problème d'histocompatibilité ce qui provoque un arrêt de la division de l'embryon d'où la nécessité d'avoir une mère porteuse ayant un patrimoine génétique le plus proche possible du donneur de cellule (et donc de la même espèce).
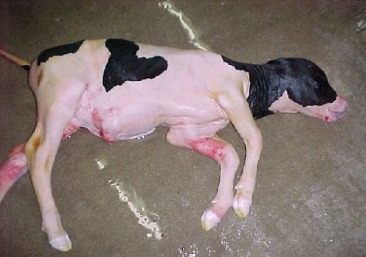
Enfin, il convient d'évoquer ce qui semble être, à l'heure actuelle, l'une des limites les plus importantes du clonage somatique : le "Large Offspring Syndrome" également appelée maladie du gros veau. L'apparition de ce syndrome serait en relation avec la teneur des produits présents lors de la culture in vitro de l'embryon ( après le choc électrique) et notamment de la teneur élevée en hormones de croissance. Il est caractérisé avant la naissance par un développement placentaire anormal : certains organes du foetus grossissent trop vite et le squelette de celui ci est déformé. On observe également une gestation prolongée de la mère porteuse qui a pour effet de faire grossir le veau plus longtemps que la normale.Cependant, le pire est à venir, en effet à sa naissance ce "gros veau" aura un masse d'environ 30 % supérieur par rapport à un veau nouveau né "normal" (60 kilos contre 40 à 45 ), certains de ces organes seront atrophiés , son squelette sera déformé, il souffrira d'hypertension, aura des problèmes cardio-vasculaires et son système immunitaire sera peu efficace contre les infections.
Veau mort né atteint du syndrome du gros veau
Vous pouvez comparer ce veau avec un veau "normal" (photo ci-dessous).
Ce syndrome du gros veau est ainsi responsable dans 33% des cas de morts postnatales chez les bovins clonés, sachant que lorsqu' ils ne meurent pas à la naissance, ces veaux sont atteints entre autre d'anémie (maladie dûe à un manque d'hémoglobine) ou meurent de problèmes cardiaques ou pulmonaires comme détaillé infra. Ce syndrome ne pouvant être traité, dès qu'il est décelé-c'est à dire dès qu'il apparaît entre le deuxième et le troisième trimestre de gestation-la porteuse est abattue.
Le clonage est donc une technique encore loin d'être au point qui rencontre des problèmes majeurs lesquelsi peuvent cependant être surmontés (ils le seront probablement dans le futur).Après tout comme le dit l'adage "Fit faber fabricando" , ces problèmes ne seront dépassés qu'avec un travail poussé des chercheurs, ce qui permettra peut être un jour de maîtriser tous les facteurs d'échecs du clonage.